Про знаменитості
Сванте серпня Арреніус: біографія
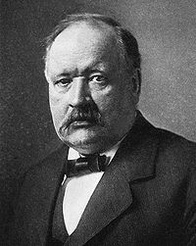
19 лютого 1859 - 02 жовтня 1927
видатний шведський фізико-хімік і астрофізик, лауреат Нобелівської премії з хімії
Ранні роки життя
Арреніус був другим сином Кароліни Христини (Тунберг) і Сванте Густава Арреніуса, що управляє маєтком. Через рік після народження сина сім'я переїхала в Уппсали, де Арреніус увійшов до складу ради інспекторів Уппсальского університету. Будучи маленькою дитиною, Арреніус уже з задоволенням складав числа в звітах, що складав його батько, у три роки самостійно навчився читати, а відвідуючи кафедральне училище в Уппсале, він проявив виняткові здібності до біології, фізики та математики.
Освіта
У 8 років Арреніус поступив в кафедральне училище в Уппсале, яке закінчив у 1876 році. У тому ж році він вступив до Упсальський університет (спеціалізувався у фізиці й хімії), де в 1878 році отримав ступінь бакалавра природничих наук, а потім протягом ще трьох років продовжував вивчати там фізику. У 1881 переїхав до Стокгольма і продовжив навчання у Фізичному інституті Королівської шведської Академії Наук під керівництвом фізика Еріка Едлунд. Там Арреніус спеціалізувався у вивченні провідності електролітів.
Під час цих досліджень він звернув увагу на той факт, що провідність розчинів при розведенні збільшується. Подальші дослідження привели його до формулювання теорії про електролітичної дисоціації, яка тепер називається теорією Арреніуса. До того часу вже давно був відомий розпад електролітів на іони при електролізі, новизна теорії Арреніуса була в тому, що він припустив розпад (дисоціацію) електролітів у розчинах за відсутності будь-яких зовнішніх сил. Арреніус написав стопятідесятістранічную дисертацію, яку представив до захисту в 1884 в Упсальський університеті. Новизна і удавана парадоксальність його ідеї про можливість одночасного існування в розчинах електролітів різнойменно заряджених іонів призвела до неприйняття теорії вченою радою, в результаті Арреніус при захисті дисертації отримав саму нижчу, четверту ступінь, яка не давала можливості викладати.
Наукова діяльність
Незважаючи на те, що в Швеції теорію Арреніуса взяли більш ніж прохолодно, багато європейських вчені їй зацікавились, особливо знаменитий німецький хімік Вільгельм Оствальд, який навіть відвідав Арреніуса в Уппсале і запросив працювати в Ризькому університеті. Хоча Арреніус відхилив пропозицію Оствальда (в цей час його батько був дуже хворий і помер в 1895), підтримка останнього допомогла йому стати лектором в Упсальський університеті. Теорія Арреніуса допомогла Оствальд вивести закон розведення, названий його ім'ям.
У 1886 Арреніус одержав стипендію Шведської королівської академії наук, це дозволило йому зробити наукове турне по Європі. У 1886 він працював спільно з Оствальдом в Ризькому політехнічному університеті, з Фрідріхом Кольраушем в 1886-1887 Вюрцбурзі (тут він зустрівся з Вальтером Нернстом) і в Грацському університеті з Людвігом Больцманом, в 1888 - в Амстердамському університеті у Я.Вант-Гоффа.< / p>
У 1887 остаточно сформулював теорію електролітичної дисоціації, в 1887 пояснив відступ розчинів електролітів від законів Вант-Гоффа і закон Рауля (показав фізичний зміст поправочного коефіцієнтаi). Створив вчення про ізогідрічності, розробив теорію гідролізу солей. Встановив екзотермічний характер більшості процесів дисоціації електролітів і залежність швидкості і повноти протікання цих процесів від температури. Займаючись хімічної кінетикою, Арреніус зробив кілька важливих відкриттів, таких, як пояснення (1889) температурної залежності швидкості реакцій, висунувши подання про активні, володіють надлишкової енергією і здатних вступати в хімічну взаємодію молекулах, число яких експоненціально зростає із зростанням температури. Ввів поняття енергії активації EАі вивів рівняння залежності константи швидкості реакції від фактора частоти зіткнення молекул A, температури і EА, що стало одним з основних в хімічній кінетиці (рівняння Арреніуса) .
← предыдущая следующая →
Cторінки: 1 2

